Phản ứng K + C6H5OH → C6H5OK + H2
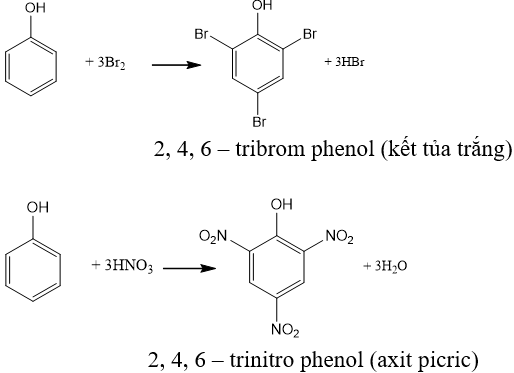
1. Phản ứng hóa học
2K + 2C6H5OH → 2C6H5OK + H2
2. Điều kiện phản ứng
Không cần điều kiện.
3. Cách thực hiện phản ứng
Cho kali tác dụng với phenol.
4. Hiện tượng nhận biết phản ứng
K tan dần trong và có khí thoát ra.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của K (Kali)
Trong phản ứng trên K là chất khử.
5.2. Bản chất của C6H5OH (Phenol)
- Trong phản ứng trên C6H5OH là chất oxi hoá.
- C6H5OH có tính axit yếu có phản ứng với các kim loại kiềm, dung dịch bazo.
6. Tính chất hoá học của K
Kali là kim loại kiềm có tính khử rất mạnh.
K → K+ + 1e
6.1. Tác dụng với phi kim
6.2. Tác dụng với axit
2K + 2HCl → 2KCl + H2.
6.3. Tác dụng với nước
K tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
6.4. Tác dụng với hidro
Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 - 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
7. Tính chất vật lí của K
Kali là kim loại nhẹ thứ hai sau liti, là chất rắn rất mềm, dễ dàng cắt bằng dao và có màu trắng bạc. - Kali bị ôxi hóa rất nhanh trong không khí và phải được bảo quản trong dầu mỏ hay dầu lửa. - Có khối lượng riêng là 0,863 g/cm3; có nhiệt độ nóng chảy là 63,510C và sôi ở 7600C.
8. Tính chất hóa học của Phenol
Nhân hút e, -OH đẩy e.
8.1. Phản ứng thế nguyên tử hiđro của nhóm OH
* Tác dụng với kim loại kiềm:
C6H5OH + Na → C6H5ONa (Natri phenolat) + 1/2 H2↑
* Tác dụng với bazơ:
C6H5OH (rắn, không tan) + NaOH → C6H5ONa (tan, trong suốt) + H2O
→ Phenol có tính axit, tính axit của phenol rất yếu; dung dịch phenol không làm đổi màu quỳ tím.
Chú ý: tính axit yếu, không làm đổi màu quỳ tím, thứ tự: nấc II của H2CO3 < phenol < nấc I của H2CO3.
⇒ Có phản ứng:
C6H5ONa (dd trong suốt) + H2O + CO2 → C6H5OH (vẩn đục) + NaHCO3
C6H5OH + Na2CO3 → C6H5ONa + NaHCO3
8.2. Phản ứng thế nguyên tử hiđro của vòng benzen
+ Phản ứng với H2:
+ Phản ứng trùng ngưng với fomandehit:
9. Câu hỏi vận dụng
Câu 1. Ở dạng lỏng, phenol và ancol benzylic đều phản ứng với
A. dung dịch NaCl.
B. dung dịch NaHCO3.
C. dung dịch NaOH.
D. kim loại K.
Lời giải:
Đáp án D
Phương trình hóa học:
2K + 2C6H5OH → 2C6H5OK + H2
2C6H5CH2OH + 2K → 2C6H5CH2OK + H2
Câu 2. Phenol phản ứng được với tất cả các chất trong dãy nào sau đây?
A. H2SO4; NaOH; NaHCO3.
B. K; Br2; CH3COOH.
C. K; NaOH; (CH3CO)2O.
D. Br2; HCl; KOH.
Lời giải:
Đáp án B
Phương trình hóa học:
2K + 2C6H5OH → 2C6H5OK + H2
2NaOH + 2C6H5OH → 2C6H5ONa + H2O
C6H5OH + (CH3CO)2O → C6H5OCOCH3 + CH3COOH
Câu 3. Cho m g K tác dụng với 9,4 g phenol phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 3,9 g B. 0,39 g
C. 1,95 g D.0,195 g
Lời giải:
Đáp án A
Phương trình hóa học: 2K + 2C6H5OH → 2C6H5OK + H2
nK = nC6H5OH = 0,1 mol
Khối lượng muối: m = 0,1.39 = 3,9 g
Xem thêm các phương trình phản ứng hóa học khác:
K2O + CO2 → K2CO3
K2O + SO2 → K2SO3
K2O + HCl → KCl + H2O
K2O + H2SO4 → K2SO4 + H2O
K2O + HNO3 → KNO3 + H2O