
Khi học hoá, CaCl2 + HCl là một phản ứng thường gặp. Cùng tìm hiểu chi tiết về phương trình hoá học, cách cân bằng cũng như đặc điểm, ứng dụng thực tế của nó nhé. Viet Chem sẽ giúp bạn có nhiều thông tin hữu ích về phản ứng này cũng như hoá học nói chung đấy.
1. Tìm hiểu về CaCl2 và HCl
1.1. CaCl2 là gì?
CaCl2 là công thức hoá học của Canxi clorua hay một số tài liệu cũng gọi nó là clorua canxi. Đây là hợp chất ion của canxi và clo, có khả năng tan nhiều trong nước với tính hút ẩm cao. Trong điều kiện nhiệt độ thường, nó là một chất rắn.

Ảnh 1: CaCl2 là công thức của Canxi Clorua - một chất có tính ứng dụng cao trong đời sống
Ngoài tên gọi chính thức, canxi clorua còn được biết với các tên sau:
- Canxi bột
- Canxi cục
- Calcium Chloride
- Canxi Diclorua
- Calcium Dichloride
- Chloride
- E509
Trong hoá học, Canxi Clorua được xem như một nguồn quan trọng để cung cấp ion canxi trong dung dịch. Do nó có thể kết tủa, nhiều hợp chất của canxi sẽ không hoà tan trong nước.
1.2. HCl là gì?
HCl là công thức hoá học của acid hydrochloric. Nó còn được biết đến với tên gọi thông dụng khác là acid muriatic. Đây là một axit vô cơ mạnh, được tạo ra từ sự hoà tan của khí hidro chloride trong nước.
Trong thực tế, Acid này có nồng độ cao nhất là 40%. Ở dạng đậm đặc, nó có thể tạo thành sương mù acid, thậm chí là ăn mòn các mô con người. Đã có những trường hợp ghi nhận về tình trạng tổn thương hô hấp, da, mắt và ruột vì tiếp xúc với axit này nồng độ cao.
2. Phản ứng CaCl2 + HCl sản phẩm là gì?

Ảnh 1: HCl và CaCl2 không thể phản ứng được với nhau
Cách thức thực hiện phản ứng này là cho khí HCl tác dụng với CaCl2. Tuy nhiên trong thực tế, phản ứng này không xảy ra. Nguyên nhân là do chúng cùng có gốc Cl nên không thực hiện được phản ứng trao đổi như quy luật.
3. Tìm hiểu về phản ứng tạo ra CaCl2 từ HCl
3.1. Phương trình phản ứng
Trong thực tế, chúng ta chỉ thường gặp phản ứng tạo ra CaCl2 với thành phần phản ứng là HCl mà thôi. Chúng ta có thể thấy phương trình của phản ứng này như sau:
Ca(OH)2 + HCl → CaCl2 + H2O
Đây là 1 phản ứng trao đổi, trong đó vôi tôi (Calcium hydroxide) tác dụng với acid hydrochloric để tạo thành hợp chất vô cơ CaCl2 - muối của canxi và clo. Và sản phẩm phụ của phản ứng này là nước.
3.2. Ứng dụng của phản ứng tạo ra CaCl2 là gì?
CaCl2 là sản phẩm chính của phản ứng. Trong tự nhiên, chất này có tính hút ẩm tự nhiên. Chính vì vậy để sử dụng lâu dài nó phải được bảo quản trong hộp kín.
Canxi Chloride có những tính chất đặc trưng như sau:
- Dạng bột màu trắng, không mùi
- Tan nhiều trong nước với một phản ứng toả nhiệt cao
- Dung dịch có vị mặn đắng gắt
- Ở dạng lỏng nó nóng chảy có thể điện phân để tạo ra kim loại canxi
- Nhiệt độ nóng chảy của nó là từ 772 đến 782 độ
- Nhiệt độ sôi là hơn 1600 độ C
- Tỷ trọng khoảng 2152 - 2512 kg/m3

Ảnh 3: Phản ứng điều chế CaCl2 được chú ý vì tình ứng dụng cao của nó
Do những tính chất đặc trưng, nó được ứng dụng trong nhiều lĩnh vực như sau:
Ứng dụng của CaCl2 trong các cơ sở sản xuất thực phẩm
Calcium Chloride là một chất phụ gia, đã được phê duyệt sử dụng ở nhiều nơi trên thế giới. Thông thường, nó được dùng trong quá trình lên men thực phẩm muối chua để tạo độ giòn và vị mặn vừa phải, không gắt trong các loại rau củ quả muối xổi, ngâm chua, muối nén…
Ngoài ra, có thể tìm thấy CaCl2 trong các loại đồ uống chuyên dùng để bổ sung chất điện giải. Nổi bật nhất là các loại nước uống thể thao, được khuyên dùng cho vận động viên, những người hoạt động nặng, người ốm mất cân bằng điện giải…

Ảnh 4: CaCl2 được dùng nhiều trong ngành thực phẩm, các sản phẩm muối chua
Trong quá trình sản xuất một số chế phẩm của sữa, Calcium Chloride cũng được sử dụng. Nổi bật có thể kể tới ứng dụng trong quá trình đảm bảo sự cân bằng của canxi và protein khi thúc đẩy quá trình kết tủa để tạo thành phomat thành phẩm.
Ứng dụng của CaCl2 trong công nghiệp
Do đặc tính hút ẩm mạnh, toả ra nhiệt lượng lớn khi tan trong nước, CaCl2 được ứng dụng trong nhiều ngành công nghiệp của thế giới. Nổi bật có thể kể tới những ứng dụng sau của hoá chất CaCl2.
- Làm khô khi chế biến tinh bột, chất bột, đồ hộp.
- Làm khô hoá chất thể lỏng, thể khí.
- Chống đóng băng ở mặt đường.
- Làm chất chống bụi, diệt nấm mốc.
- Calcium Chloride là chất phụ gia quan trọng trong quá trình hoá dẻo, làm chất tải lạnh quan trọng của kem.
- Calcium Chloride làm tăng thời gian đông lại của bê tông thành phẩm.
- CaCl2 cũng là phụ gia để tải nhiệt, làm khô khi làm giấy.
- Có khả năng hỗ trợ thúc đẩy hiệu quả khi xử lý nước thải công nghiệp.
- Hút oxy mạnh mẽ trong không khí nên được dùng rất nhiều trong sản xuất các chất chữa cháy.
- Ở nồng độ thấp, nó dùng để pha loãng nước xả vải, đảm bảo an toàn cho cơ thể.
- Diệt cỏ trên đường sắt, làm khô và hạn chế bụi bẩn trong quá trình khoan dầu khí.
Ứng dụng của CaCl2 trong y học
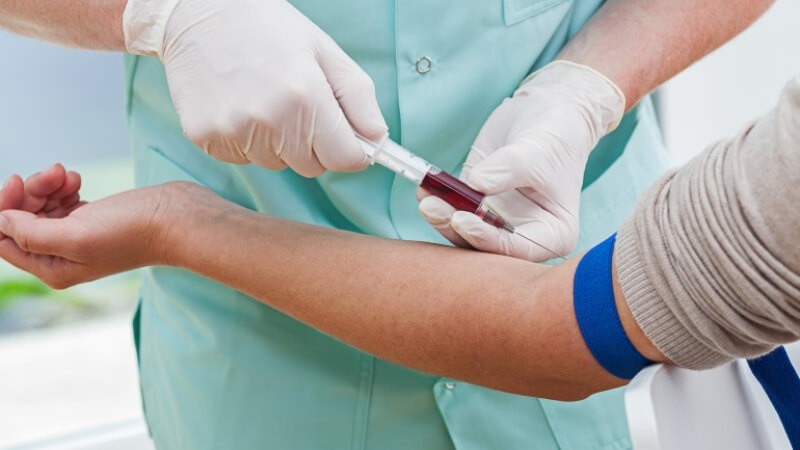
Ảnh 5: Đây cũng là một chất không thể thiếu trong y học
Hoá chất này được dùng trong việc chế tạo ra các loại thuốc tiêm, thuốc bôi điều trị côn trùng đốt hoặc làm giảm đau cho cơ thể. Tuy nhiên, thành phần, liều lượng của nó được kiểm soát rất chặt chẽ để đảm bảo hiệu quả điều trị mề đay, ngộ độc magie… Nếu không có thể gây độc nghiêm trọng cho cơ thể.
Như vậy, Vietchem đã giúp bạn tìm hiểu về CaCl2 + HCl. Hy vọng những điều do Vietchem cung cấp hữu ích với bạn. Nếu cần mua hoá chất hay tìm hiểu thêm về ngành hoá học, hãy theo dõi và liên hệ với các chuyên viên của chúng tôi để được hỗ trợ nhé.
Link nội dung: https://phamkha.edu.vn/cacl2-hcl-a10333.html